- Biología del Desarrollo
- Bioquímica y Biología Celular de Parásitos
- Bioquímica y Fisiología de la Maduración de Frutos
- Biotecnologías en Bovinos y Ovinos
- Células Madre y Terapia Génica
- Ecología Acuática
- Ecología Microbiana Ambiental
- Estrés Abiótico y Biótico en Plantas
- Fisiología y Asistencia al Mejoramiento Vegetal
- Fisiología de Plantas
- Fitobacteriología
- Fotoquímica y Fotobiología Molecular
- Ictiofisiología y Acuicultura
- Interacciones planta-microorganismos
- Micología y Cultivo de Hongos Comestibles y Medicinales
- Microbiología del Suelo
- Molecular Farming y Vacunas
- Neuroendocrinología Comparada
- Parasitología Molecular
- Parásitos Anaerobios
Laboratorio de Fotoquímica y Fotobiología Molecular
Director

- Dr. Franco M. Cabrerizo - Investigador Principal CONICET. Profesor Asociado y Coordinador de la Ingeniería en Agrobiotecnología UNSAM fcabrerizo@intech.gov.ar
Integrantes
- Dra. María Paula Denofrio - Investigadora Independiente CONICET. Profesora Adjunta UNSAM pdenofrio@intech.gov.ar

- Dra. María Micaela González- Investigadora Adjunta CONICET. Profesora Adjunta UNSAM mgonzalez@intech.gov.ar

- Dr. Ronald Vargas Balda Investigador Asistente CONICET (alta en trámite) - Profesor Adjunto UNSAM ronaldvargas@intech.gov.ar

- Dra. Lorean Madriz Investigadora Asistente CONICET (alta en trámite) - Profesora UNSAM lmadriz@intech.gov.ar
- Lic. Jesus Alberto Marquez Ramirez - Becario Doctoral ANPCyT jmarquez@intech.gov.ar
- Ingeniera Química - María Mirabal - Becaria Doctoral CONICET - amirabalcarrizo@intech.gov.
ar
Miembros anteriores - Posición actual
Dra. M. Lis Alomar (2013 – 2022)
Dr. Juan G. Yañuk (2011 – 2022)
Dr. Ivan Maisuls (2014 – 2019)
Dr. Federico Rasse-Suriani (2011 – 2016)
Dr. Damián Rodriguez (2020 – 2021)
Dra. Ivana Karina Levy (2013 – 2015)
Dra. Mariana Vignoni (2012 – 2013)
Lic. Margherita Zuccheli (2017)
Líneas de Investigación
Las β-carbolinas (βCs) comprenden una gran variedad de alcaloides naturales estructuralmente relacionados a 9H-pirido[3,4-b]indol o norharmano. Estos alcaloides están ampliamente distribuidos en especies filogenéticamente distantes entre sí (animales, plantas, insectos, etc.), incluidos organismos fototróficos. Particularmente en mamíferos, estos compuestos son partes constitutivas de órganos, tejidos y fluidos corporales (ojos, piel, plasma, orina, etc.). Como parte de un programa cuyo objetivo es comprender las bases moleculares de los procesos fotoquímicos y fotobiológicos donde estos compuestos están implicados, estudiamos las propiedades espectroscópicas, químicas y fotoquímicas más relevantes de las βCs totalmente aromáticas y de sus 3,4- dihidro-derivados (Esquema 1). Esta información relevante provee un valioso panorama para teorizar y/o establecer hipótesis sobre el rol biológico que estos compuestos podrían tener, así como también explorar diversas aplicaciones biotecnológicas.
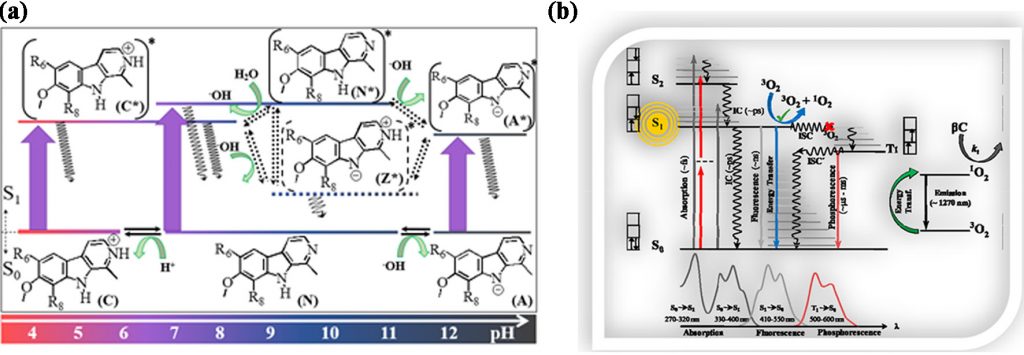
Esquema 1. (a) Ejemplos representativos de algunos compuestos estudiados (Harmina = Ha (R6 = R8 = H), 6-cloroharmina = 6-Cl-Ha (R6 = Cl and R8 = H), 8-cloroharmina = 8-Cl-Ha (R6 = H and R8 = Cl) y 6,8-dicloroharmina = 6,8-diCl-Ha (R6 = R8 = Cl)) y los distintos equilibrios ácido-base presentes en todo el rango de pH investigado. (b) Diagrama de Jablonsky modificado ilustrando los procesos fotofisicos más relevantes que siguen las βCs bajo condiciones de excitación mono y bi-fotónica.
Referencias:
[1] PHYSICAL CHEMISTRY CHEMICAL PHYSICS; 2021, vol. 23 p. 11039 – 11051
[2] PHYSICAL CHEMISTRY CHEMICAL PHYSICS; 2020, vol. 22 p. 20901 – 20913
[3] JOURNAL OF THE ARGENTINE CHEMICAL SOCIETY; 2020, vol. 107 p. 186 – 229
[4] PHOTOCHEMISTRY AND PHOTOBIOLOGY; 2018, vol. 94 p. 36 – 51
[5] PHYSICAL CHEMISTRY CHEMICAL PHYSICS; 2016, vol. 18 p. 886 – 900
[6] DALTON TRANSACTIONS; 2015, vol. 44 p. 17064 – 17074
[7] PHYSICAL CHEMISTRY CHEMICAL PHYSICS; 2015, vol. 17 p. 12090 – 12099
[8] CHEMPHYSCHEM; 2010, vol. 11 p. 796 – 798
[9] JOURNAL OF PHYSICAL CHEMISTRY A; 2009, vol. 113 p. 6648 – 6656
[10] PHOTOCHEMICAL AND PHOTOBIOLOGICAL SCIENCES; 2009, vol. 8 p. 1139 – 1149
La radiación solar induce modificaciones al ADN genómico como así también a las proteínas. Este hecho propicia, entre otros, el desarrollo de diferentes afecciones de la piel. Estas reacciones pueden ocurrir tanto por excitación electrónica directa de las biomoléculas blanco (debido a la porción UVB del espectro solar) o mediante procesos indirectos. Este último caso implica la participación de reacciones fotosensibilizadas, donde un cierto compuesto (fotosensibilizador) absorbe parte de la radiación incidente (UVA o visible) y, desde sus estados electrónicamente excitados, es capaz de desencadenar múltiples procesos que conllevan a un daño oxidativo sobre estructuras biológicas relevantes (ADN, proteínas, etc.). Poco se conoce aún acerca de la contribución de las reacciones fotosensibilizadas a la generación de cáncer de piel y otras patologías relacionadas. Y, aunque no son tan efectivos como el daño directo al ADN o a las proteínas causados por la radiación UVC y UVB, las reacciones de fotosensibilización contribuyen de manera significativa a la genotoxicidad de la radiación solar.
Existen diversos compuestos (exógenos y/o endógenos) que pueden actuar como fotosensibilizadores. En particular, las βCs representan un grupo de candidatos muy eficientes capaces de inducir daño sobre blancos biológicos relevantes (tales como el ADN) y en cultivos celulares bajo fotoexcitación (Esquema 2). Para entender en mayor profundidad los mecanismos de acción implicados en estos procesos, en nuestro grupo se estudian las propiedades fotosensibilizadoras de estos alcaloides.
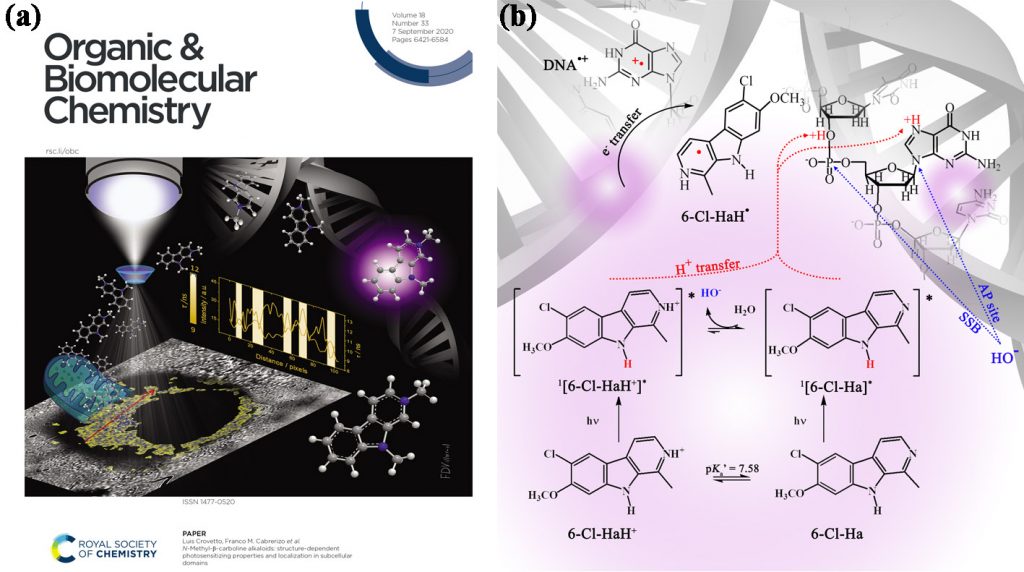
Esquema 2. (a) Tapa del número N° 33, vol 18, 2020 de la revista Organic and Biomolecular Chemistry (RSC). (b) Mecanismo de daño al ADN fotosensibilizado por 6-cloroharmina.
Referencias:
[1] ORGANIC & BIOMOLECULAR CHEMISTRY; 2020, vol. 18 p. 6519 – 6530
[2] CHEMISTRY-A EUROPEAN JOURNAL; 2018, vol. 24 p. 12902 – 12911
[3] ORGANIC & BIOMOLECULAR CHEMISTRY; 2018, vol. 16 p. 2170 – 2184
[4] JOURNAL OF PHOTOCHEMISTRY AND PHOTOBIOLOGY A-CHEMISTRY; 2018, vol. 364 p. 169 – 176
[5] JOURNAL OF PHOTOCHEMISTRY AND PHOTOBIOLOGY B-BIOLOGY; 2014, vol. 132 p. 67 – 71
[6] PHYSICAL CHEMISTRY CHEMICAL PHYSICS; 2014, vol. 16 p. 16547 – 16562
[7] ORGANIC & BIOMOLECULAR CHEMISTRY; 2013, vol. 11 p. 5300 – 5309
[8] ORGANIC & BIOMOLECULAR CHEMISTRY; 2012, vol. 10 p. 1807 – 1819
[9] ORGANIC & BIOMOLECULAR CHEMISTRY; 2012, p. 9359 – 9372
[10] ORGANIC & BIOMOLECULAR CHEMISTRY; 2010, vol. 8 p. 2543 – 2552
La terapia fotodinámica se basa en la citotoxicidad de los fotosensibilizadores en presencia de luz. La eficacia y selectividad del tratamiento se incrementa si se logra la internalización selectiva del fotosensibilizador en las células blanco (típicamente células tumorales). Con este objetivo, nuestro grupo sigue dos estrategias diferentes:
(a) Un transportador interesante para ese propósito es el receptor de ácido fólico α (FRα), que se encuentra sobreexpresado en la superficie de varios tipos de células tumorales y media la internalización endocítica. Para este fin, se trabajó sobre la síntesis y caracterización fotobiológica de βCs cuaternarias como fotosensibilizadores unidos covalentemente a albúmina conjugada con folato como sistemas transportadores. En un trabajo previo probamos que los conjugados albúmina-folato son vehículos prometedores para la terapia fotodinámica de células tumorales. Estas partículas pueden ser internalizadas selectivamente y acumuladas en los lisosomas de las células KB (carcinoma humano), y son fototóxicas bajo fotoexcitación. Sin embargo, aún se requieren nuevos desarrollos que permitan incrementar considerablemente la eficiencia de estos conjugados (Esquema 3a).
(b) Los entramados metalórganicos (MOFs, por sus siglas en inglés) representan otro grupo de nanomateriales estructurados interesantes con propiedades físico-químicas remarcables. Estas propiedades pueden ser modificadas reemplazando los núcleos metálicos o los ligandos. En el contexto de la terapia fotodinámica y el transporte de drogas, nuestro grupo está interesado en un conjunto de MOF de escala nanométrica hechos de una estructura reticular con núcleos de circonio coordinados a ligandos orgánicos fotoactivos (ZrMOF) (Esquema 3b). Este tipo de estructuras basadas en MOF proveen un marco para la organización espacial de los fotosensibilizadores, aumentando potencialmente la producción de especies reactivas de oxígeno y, al mismo tiempo, proveen una estructura porosa que permite la adsorción de compuestos de interés. Además, los materiales basados en Zr tienen la ventaja de ser biocompatibles y estables a valores bajos de pH. El programa actual tiene como objetivo optimizar las estructuras ZrMOF para su uso en terapia fotodinámica. El ajuste óptimo de los procesos de síntesis para obtener nanomateriales de tamaño controlado es primordial, dado que deben ser capaces de entrar en las células blanco y ejercer daño, mientras que el control sobre la estructura del sensibilizador es importante para evitar procesos de auto-blanqueamiento.
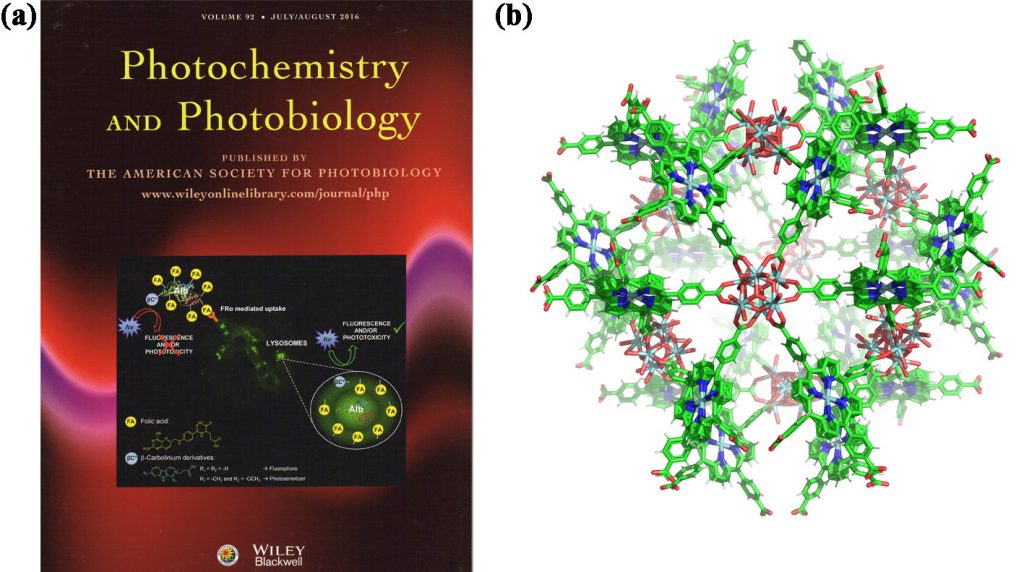
Esquema 3. (a) Tapa del número N° 4, vol 92, 2016 de la revista Photochemistry and Photobiology (Wiley Blackwell). (b) Estructura representativa de ZrMOF.
Referencias:
[1] PHOTOCHEMISTRY AND PHOTOBIOLOGY; 2016, vol. 92 p. 611 – 619.
[2] PHYSICAL CHEMISTRY CHEMICAL PHYSICS; 2015, vol. 17 p. 12462 – 12465.
[3] MICROPOROUS MATERIALS AS DRUG CARRIERS, undergraduate Thesis, Engineer Francisco Simón, 2016.
[4] 2nd prize, INNOVAR 2014 (Category: Phytomedicine) “Terapias alternativas para el tratamiento de la Tritrichomonosis bovina”.
En las últimas décadas, la resistencia a las drogas de los agentes patógenos constituye un gran problema para la salud pública a nivel global. Por lo tanto, es necesario no solamente encontrar nuevos antimicrobianos, sino también mejorar la eficacia y farmacocinética de los tratamientos actuales y nuevas estrategias de prevención de las infecciones. En este contexto, y tomando en cuenta el amplio espectro de acción anti-patogénico de las βCs, evaluamos las propiedades inhibitorias de compuestos naturales y de síntesis de esta familia contra diferentes patógenos de humanos, animales y plantas. Hasta la fecha, hemos estudiado el efecto de las βCs contra el virus del Herpes simplex Tipo I y II, Toxoplasma gondii, Penicillium digitatum y Botrytis cinerea. La síntesis de nuevas drogas incluye alquilaciones, entre otras. Los métodos de separación, purificación y caracterización de compuestos son los usados tradicionalmente en el campo de la química orgánica (extracciones líquido-líquido, técnicas cromatográficas, RMN, HPLC, análisis termogravimétrico, espectroscopía de absorción UV-vis, diferentes técnicas de espectrometría de masas, etc.) Los mecanismos subyacentes de acción de βCs son explorados a través de análisis del ciclo celular, inmunofluorescencia indirecta y ensayos western blot, producción de ERO intracelular, entre otros (Esquema 4).
Adicionalmente, usamos las propiedades fotosensibilizadoras de estos y otros compuestos relacionados para mejorar el efecto inhibitorio y/o atenuar los diferentes microorganismos con propósitos biotecnológicos.
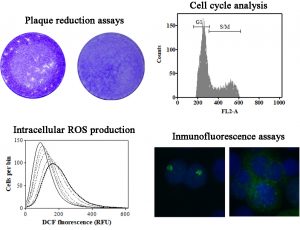
Esquema 4. Ejemplo representativo de resultados obtenidos con diferentes técnicas y metodologías de análisis usadas durante la evaluación del efecto antimicrobiano de las βCs.
Referencias:
[1] FRONTIERS IN MICROBIOLOGY; 2021, vol. 12
[2] INTERNATIONAL JOURNAL OF ANTIMICROBIAL AGENTS; 2018, vol. 52 p. 459 – 468
[3] JOURNAL OF PHOTOCHEMISTRY AND PHOTOBIOLOGY B-BIOLOGY; 2017, vol. 177 p. 8 – 17
[4] FRONTIERS IN MICROBIOLOGY; 2017, vol. 8
[5] FOOD MICROBIOLOGY; 2017, vol. 62 p. 9 – 14
[6] BMC RESEARCH NOTES; 2013, vol. 6 p. 193 – 198
En plantas, las βCs constituyen un gran grupo de alcaloides indólicos ampliamente distribuidos en diferentes especies incluyendo Peganum harmala (Zygophillaceae), Banisteriopsis capii, Leguminoseae, Malpighiaceae, Passifloraceae, entre otras. En la actualidad, la información concerniente a la biosíntesis de las βCs es aún incompleta y, los procesos químicos involucrados necesitan ser comprendidos en profundidad. La formación de tetrahidro-βCs implicaría una condensación catalizada mediante la vía Pictet-Spengler desde los triptófanos y aldehídos. El tipo y número de enzimas implicadas en este proceso difiere de un organismo al otro. En las plantas, la estrictosidina sintasa (STR) cataliza las reacciones de condensación entre triptamina y secologanina para dar lugar a la formación de los correspondientes tetrahidro-derivados de βCs. El esqueleto tetrahidro-derivado puede, además, ser modificado dando lugar a la formación de una gran variedad de derivados (tales como dihidro-, epoxi-, ceto, hidroxi-), incluyendo la formación de βCs completamente aromáticas, ampliamente distribuidas en todos los organismos vivos. La formación de estos compuestos puede ocurrir a través de procesos enzimáticos o no enzimáticos. En este sentido, tomando en cuenta la presencia de estos alcaloides en órganos aéreos expuestos a la radiación solar (hojas, tallos y otros), las vías fotoquímicas (Esquema 5) deberían ser investigadas en mayor profundidad como una vía adicional de oxidación no enzimática y/o aromatización completa de los tetrahidro-derivados de βCs (Esquema 5).
En relación a las funciones biológicas de estos alcaloides, se sugirió que en las plantas tendrían un papel clave en el mecanismo de defensa contra agentes invasores. Sin embargo, aún no se conocen las bases moleculares de los mecanismos de acción. Además, y teniendo en cuenta la muy variada respuesta fotoquímica que muestran las βCs, se espera su participación en otro tipo de procesos. Esto pone de manifiesto la necesidad de llevar adelante estudios que permitan dilucidar el papel que juegan estos alcaloides en las plantas.
En este contexto, las investigaciones que actualmente se llevan a cabo en nuestro grupo de trabajo buscan evaluar el tipo de modificaciones metabólicas que desencadena el estrés lumínico (UVB, UVA y luz azul) en el modelo de planta de soja, conjuntamente con el rol protector de las βCs. El seguimiento de la respuesta al estrés incluye medidas de actividad enzimática, determinación de diferentes parámetros asociados al crecimiento de la planta. Mediante el uso de técnicas espectroscópicas (UV-vis y fluorescencia en estado estacionario), combinadas con el análisis quimiométrico (MCR y PARAFAC) se evaluar la evolución de la concentración de los pigmentos vegetales (clorofilas, antocianinas y carotenoides).
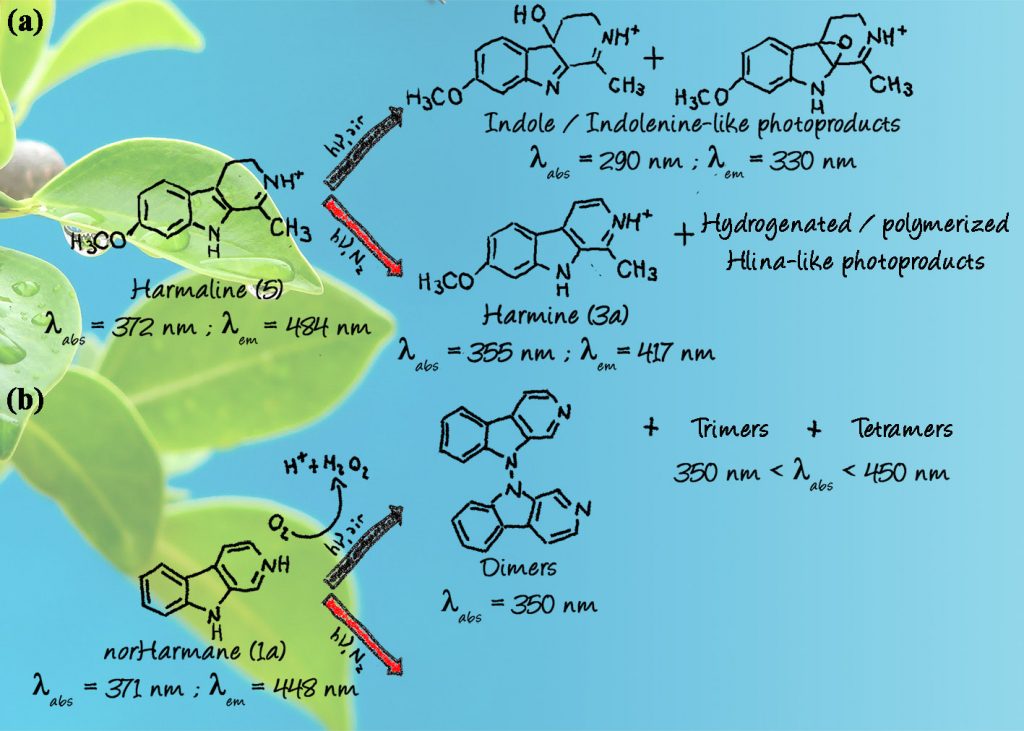
Esquema 5. Representación de las principales vías de degradación fotoquímica de: (a) Harmalina y (b) Harmina.
Referencias:
[1] JOURNAL OF PHOTOCHEMISTRY AND PHOTOBIOLOGY B-BIOLOGY; 2019, vol. 199
[2] PHOTOCHEMICAL AND PHOTOBIOLOGICAL SCIENCES; 2009, vol. 8 p. 1139 – 1149
Esta línea de investigación se centra en comprender aspectos fundamentales de los procesos redox (Esquema 6). Los cuatro objetivos específicos están dirigidos a:
(a) Profundizar en las reacciones de transferencia de oxígeno por vía fotoelectroquímica, que es la base de uno de los procesos de oxidación avanzada que utiliza la luz solar para lograr la remediación de aguas residuales.
(b) Explorar el potencial de los procesos de electrocristalización para formar nuevas fases, que puedan catalizar reacciones relacionadas con tecnologías renovables basadas en hidrógeno y/o reducción de sustancias inorgánicas, como nitratos e iones metálicos.
(c) En fotocatálisis, se busca avanzar en el uso de semiconductores nanoestructurados para oxidar la materia orgánica presente en cuerpos de agua con la generación concomitante de combustibles solares mediante acoplamiento de una reacción de reducción adecuada. Permitiendo así, el desarrollo de habilidades en tecnologías de la nueva era que utilizan la energía solar para promover reacciones químicas. Se investiga continuamente el papel de las propiedades optoelectrónicas de los electrodos semiconductores que se aplican para llevar a cabo la reacción de división del agua y la oxidación de compuestos químicos seleccionados.
(d) Desarrollar metodologías electroanalíticas para la detección y cuantificación de moléculas de interés ambiental y agroindustrial.
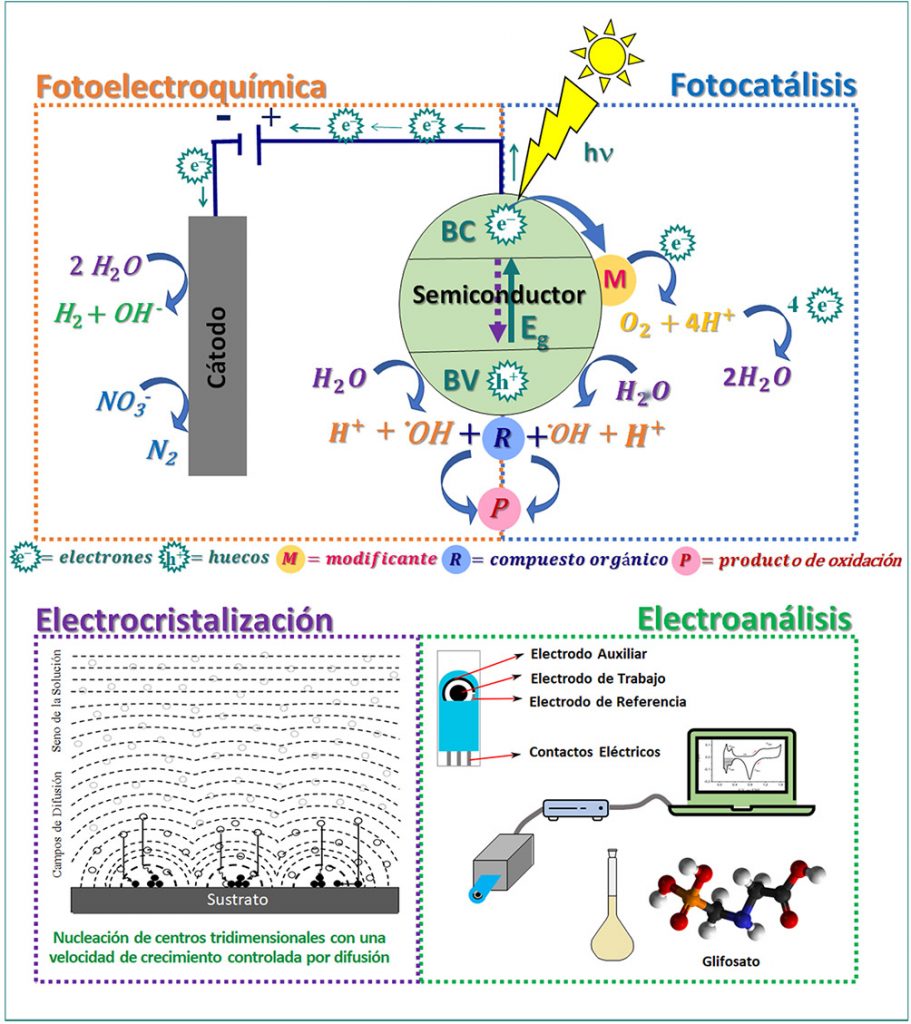
Esquema 6. Resumen gráfico de los principales procesos electroquímicos, reacciones y metodologías usadas en el marco de las investigaciones descriptas en esta sección.
Referencias:
[1] JOURNAL OF PHYSICAL CHEMISTRY C; 2021, vol. 125 p. 610 – 617
[2] JOURNAL OF PHYSICAL CHEMISTRY C; 2021, vol. 125 p. 12682 – 12689
[3] ENERGY REPORTS; 2020, vol. 6 p. 25 – 36
[4] RENEWABLE ENERGY; 2020, vol. 152 p. 974 – 983
[5] SPECTROCHIMICA ACTA. PART A, MOLECULAR & BIOMOLECULAR SPECTROSCOPY.; 2017, vol. 176 p. 91 – 98
Publicaciones
Hojamberdiev M, Vargas R, Madriz L, Nematov, D, Shaislamov U, Wagata H, Kubota Y, Yubuta K, Teshima K, Matsushita N. Tuning optoelectronic properties and photoelectrochemical performance of β-TaON via vanadium doping. Small 0:e10276. 2026. https://doi.org/10.1002/smll.202510276
Castañeta G, Miranda-Flores D, Bustos AS,f García R, Loayza E, Carrasco C, Tejeda L, Cabrerizo FM, Peñarrieta JM. Influence of sunlight exposure and traditional dehydration on chemical and nutritional properties of Oxalis tuberosa (oca) Tubers. Plant Foods for Human Nutrition 80, 91. 2025. https://doi.org/10.1007/s11130-025-01330-x
De Gerónimo E, Mosca A, Cabrerizo FM, Vargas R. Insights into chlorination-induced degradation of sulfonylurea herbicides: Unraveling kinetics and intermediates during water treatment. Water Research 280, 123513. 2025. https://doi.org/10.1016/j.watres.2025.123513
Glez S, Carrasco C, Böök O, Castañeta G, Loayza E, Peñarrieta JM, Pepova T, Cabrerizo FM, Tejeda L, A comprehensive analysis of the nutritional value, antioxidant potential and fatty acid composition of lucuma (Pouteria lucuma) fruit, grown in the high-altitude valleys of Bolivia. Anais da Academia Brasileira de Ciências 24, 97. 2025. doi: https://doi.10.1590/0001-3765202520241017
Madriz l, Márquez J, González MM, Denofrio MP, De Gerónimo E, Dell’Arciprete ML, Vargas R, Cabrerizo FM. Electroanalytical and spectroscopic approaches combined with photo (electro)catalytic treatment for real-time decision-making on rural groundwater quality. Journal of Water Process Engineering 77, 108630. 2025. https://doi.org/10.1016/j.jwpe.2025.108630
Rasse-Suriani FAO, Alves Costas R, Denofrio MP, García Einschlag FS, Cabrerizo FM. Interaction of normelinonine F and related N-methyl-β-carbolines derivatives with bovine serum albumin. Spectroscopic profiles, multivariate analysis and theoretical calculation. International Journal of Biological Macromolecules 299, 140136, 2025. https://doi.org/10.1016/j.ijbiomac.2025.140136
Saldarriaga Cartagena AM, Aparicio Arias A, Cristaldi C, Ganuza A, Gonzalez MM, Corvi MM, Sullivan WJ Jr, Vanagas L, Angel SO. Toxoplasma gondii RAD51 recombinase is required to overcome DNA replication stress and its inactivation leads to bradyzoite differentiation. DNA Repair (Amst) 152, 103882, 2025. https://doi.org/10.1016/j.
González MM, Vizoso-Pinto MG, Erra-Balsells R, Gensch T, Cabrerizo FM. Article In Vitro Effect of 9,9′-Norharmane Dimer against Herpes Simplex Viruses. International Journal of Molecular Sciences 25, 4966. 2024. https://doi.org/10.3390/ijms2509496
Hojamberdiev M, Vargas R, Madriz L, Kadirova ZC, Yubuta K, Zhang F, Teshima K, Lerch M. Untangling the effect of carbonaceous materials on the photoelectrochemical performance of BaTaO2N. ACS Omega 9, 6, 7022-7033.2024. https://doi.org/10.1021/acsomega.3c08894
Márquez V, Ng E, Torres D, Borrás C, Scharifker BR, Cabrerizo FM; Madriz L, Vargas R. Chapter in “Advances in Catalyst Research”. Electrochemical approach for hydrogen technology: fundamental concepts and materials. Edit: Springer Cham, 339-376. 2024. https://doi.org/10.1007/978-3-031-49108-5_10
Ospina-Calvo B, De Gerónimo E, Villarruel FD, Aparicio VC, Ashworth L, Erra-Balsells R, Cabrerizo FM. Distribution of photoactive β-carboline alkaloids across Passiflora caerulea floral organs. Photochemistry and Photobiology 100, 87-100. 2024. https://doi.org/10.1111/php.
Ragone F, Yanuk JG, Cabrerizo FM, Prieto E, Wolcan E, Ruiz GT. DNA structural changes (photo)induced by tricarbonyl (pterin)rhenium (I) complex. Journal of Inorganic Biochemistry 252, 112471. 2024. https://doi.org/10.1016/
Ramzan M, Raza A, un Nisa Z, Abdel-Massih RM, Al Bakain R, Cabrerizo FM, Dela Cruz TE, Aziz RK, Musharraf SG. Detection of antimicrobial resistance (AMR) and antimicrobial susceptibility testing (AST) using advanced spectroscopic techniques: A review. TrAC Trends in Analytical Chemistry 172, 117562. 2024. https://doi.org/10.1016/j.trac.2024.117562
Vargas R, Méndez D, Torres D, Carvajal D, Cabrerizo F, Madriz L. Simultaneous p-nitrophenol remediation and hydrogen generation via dual-function photoelectrolytic cell: P-TiO2 photoanode and CuP cathode International Journal of Hydrogen Energy 59, 159-167. 2024. https://doi.org/10.1016/j.ijhydene.2024.01.303
Villarruel FD, Denofrio MP, Schmidt de León T, Erra-Balsells R, Wolcan E, García Eincschlagd FS, Cabrerizo FM. Exploring photooxidative degradation pathways of harmol and harmalol alkaloids in water: effects of pH excitation sources and atmospheric conditions. Physical Chemistry Chemical Physics. En prensa. https://doi.org/10.1039/D3CP05223K
Zhu H, Cabrerizo FM, LI J, He T, Li Y. Rewiring photosynthesis by water-soluble fullerene Derivatives for solar-powered electricity generation. .Advanced Science 2310245. 2024. https://doi.org/10.1002/advs.202310245
Apuzzo E, Agazzi M, Herrera SE, Picco A, Rizzo G, Chavero C, Bianchi D, Smaldini P, Cortez ML, Marmisollé WA, Padula Gm Seoane A, Alomar ML, Denofrio MP, Docena G, Azzaroni O. Poly(allylamine)-tripolyphosphate ionic assemblies as nanocarriers: friend or foe?. ACS Applied Bio Materials 6,11, 4714-4727. https://doi.org/10.1021/acsabm.3c00489
Cabrerizo FM. A boost for south–south collaboration. Nature 616, 249. 2023. https://doi.org/10.1038/
Denofrio MP, Paredes JM, Yañuk JG, Giron MD, Salto R, Talavera EM, Crovetto L, Cabrerizo FM. Photosensitizing properties and subcellular localisation of 3,4-dihydro-β-carbolines harmaline and harmalol. Photochemical & Photobiological Sciences 22, 488-501. 2023. https://doi.org/10.1007/
dos Santos AJ, Barazorda-Ccahuana HL, Caballero-Manrique G, Chérémond Y, Espinoza-Montero PJ, Jáuregui-Haza UJ, Lanza MRV, Nájera A, Oporto C, Pérez Parada A, Pérez T, Delgado Quezada V, Rojas V, Sosa V, Thiam A, Torres-Palma RA, Vargas R, García Segura S. Accelerating innovative water treatment in Latin America. Nature Sustainability 6, 349-351. 2023. https://doi.org/10.1038/s41893-022-01042-z
Gómez Velázquez Laura S, Dell’Arciprete María L, Madriz Lorean, González Mónica C. Carbon nitride from urea: Mechanistic study on photocatalytic hydrogen peroxide production for methyl orange removal. Catalysis Communications 175, 106617. 2023. https://doi.org/10.1016/j.catcom.2023.106617
Gómez-Velázquez LS, Madriz L, Rigoletto M, Laurenti E, Bizarro M, Dell’ Arciprete ML, González M. Structural and physicochemical properties of Carbon Nitride nanoparticles via precursor thermal treatment: effect on methyl orange photocatalytic discoloration. ACS Publications Nano Materials 6, 14049-14062. 2023. https://doi.org/10.1021/acsanm.3c01935
Hojamberdiev M, Larralde AL,Vargas R, Madriz L, Yubuta K, Sannegowda LK, Sadok I, Krzyszczak-Turczyn A, Oleszczuk P, Czech B. Unlocking the effect of Zn2+ on crystal structure, optical properties, and photocatalytic degradation of perfluoroalkyl substances (PFAS) of Bi2WO6. Environmental Science: Water Research and Technology 9, Pages 2866 – 28796. 2023. https://doi.org.10.1039/d3ew00430a
Hojamberdiev M, Vargas R, Zhang F, Teshima K, Lerch M. Perovskite BaTaO2N: From materials synthesis to heterogeneous solar water splitting. Advance Science 2305179. 2023. https://doi.org/10.1002/advs.202305179
Madriz L, Cabrerizo FM, Vargas R. Electrochemical studies on β-carbolines alkaloids: Kinetics of irreversible oxidation processes. Electrochimica Acta 464, 142918. 2023. https://doi.org/10.1016/j.electacta.2023.142918
Nuñez O, Vargas R. Chapter 8: The interplay between RedOx, photophysics and surface process in Bi2WO6 photocatalyst. En «A Closer Look at Chemical Kinetics Chemistry». Editado por: Victor Martinez-Luaces. Nova Science Publishers 206-222. 2023. https://d0i:10.52305/GLSO9660
Vargas R, Madriz L, Vilar VJP, Fatta-Kassinos D. Updating the difficulties of the Venezuelan scientific work. Journal of Environmental Chemical Engineering 11, 109579. 2023. https://doi.org/10.1016/j.jece.2023.109579
Espinoza-Montero P, Vargas R, Alulema-Pullupaxi P, Fernández L. Advanced Oxidation Processes for Wastewater Treatment: An Innovative Approach. En “Photoelectrocatalysis: Principles and Applications”. Editado por Shah mP, Bera SP, Tore GY. CRC Press, Boca Ratón, Florida, USA. pp 53-68. 2022. https://doi.org/10.1201/978100
Hojamberdiev M, Czech B, Wasilewska A, Boguszewska-Czubara A, Yubuta K, Wagata H, Daminova S, Kadirova Z, Vargas R. Detoxifying SARS-CoV-2 antiviral drugs from model and real wastewaters by industrial waste-derived multiphase photocatalysts. Journal of Hazardous Materials 429, 128300. 2022. https://doi.org/10.1016/j.jhazmat.2022.128300
Hojamberdiev M, Mora-Hernández J M, Vargas R, Heppke EM, Yubuta K, Yamakata A, Kadirova Z, Torres-Martínez L, Teshima K, Lerch M. Eliciting the contribution of TiN to photoelectrochemical performance enhancement of Imma-LaTiO2N at neutral pH. Materials Today Energy, 27, 101053. 2022. https://doi.org/10.1016/j.mtener.2022.101053
Hojamberdiev M, Vargas R, Daminova S, Kadirova Z. Understanding the photodegradation mechanism of gaseous acetaldehyde over BI2W06-modified ZNW04 photocatalyst under UV light irradiation. Chemistry and Chemical Engineering 2021, 4, 9. 2022. https://doi.org/10.
Hojamberdiev M, Vargas R, Kadirova Z, Teshima K, Lerch M. Exploring the Effect of B-Site Al3+-Mg2+ + Dual Substitution on Optoelectronic, Surface, and Photocatalytic Properties of BaTaO2N. Materials Advances. En prensa. https//doi.org/10.1039/D2MA00611A
Hojamberdiev M, Vargas R, Kadirova ZC, Kato K, Sena H, Krasnov AG, Yamakata A, Teshima K, Lerch M. Unfolding the role of B site-selective doping of aliovalent cations on enhancing sacrificial visible light-induced photocatalytic H2 and O2 evolution over BaTaO2N. American Chemical Society Catalysis 12, 1403-1404. 2022. https://doi.org/10.1021/
Otuechere CA, Adewuyi A, Ekozin A, Feng X, Cabrerizo FM. Green synthesized zinc oxide nanoparticles elicited a prominent suppression of oxidative and inflammatory distortions in rats exposed to carbon tetrachloride. Biointerface Research in Applied Chemistry 12, 5444-5457. 2022. https://doi:10.33263/BRIAC124.54445457
Vargas R, Madriz L, Marqueza V, Torres D, Kadirova ZC, Yubuta K, Hojambnerdiev M. Elucidating the enhanced photoelectrochemical performance of zinc-blende ZnS/wurtzite ZnO heterojunction and adsorption of water molecules by molecular dynamics simulations. Materials Science in Semiconductor Processing 142, 106494. 2022. https://doi.org/10.1016/j.mssp.2022.106494
Hojamberdiev M, Vargas R, Bhatu VS, Torres D, Kadirova ZC, Kumar M. Unraveling photoelectrochemical behavior of Ni-modify ZnO and TiO2 thin films fabricated by RF magnetron sputtering. Journal of Electroanalytical Chemistry. 882, 115009. 2021. https://doi.org/10.1016/j.jelechem.2021.115009
Leon D, Maimone A, Carvajal D, Madriz L, Scharifker BR; Cabrerizo FM, Vargas R. Unraveling kinetic effects during photoelectrochemical mineralization of phenols. Rutile: anatase TiO2 nanotube photoanodes under thin-layer conditions. Journal of Physical Chemistry C 125, 610–617. 2021. https://doi.org/10.1021/acs.jpcc.0c09890
Madriz L, Cabrerizo FM, Vargas R. Exploring chemical kinetics at home in times of pandemic: following the bleaching of food dye allura red using a Smartphone. Journal of Chemical Education 98, 6, 2117–2121. 2021. https://doi.org/10.
Madriz L, Parra M, García Einschlag FS, Núñez O, Cabrerizo FM, Vargas R. Photocatalytic Oxidation of Urea on Surface-Modified Bi2WO6 with trans-4-Stilbenecarboxaldehyde. Journal of Physical Chemistry C. 125, 12682-12689. 2021. https://doi.org/10.1021/acs.jpcc.1c03063
Rueda H, Arenas M, Vargas-Balda R, Blanco S, Delvasto P. Production of a nickel-based catalyst for urea electrooxidation using spent batteries as raw material: Electrochemical synthesis and implications from a circular economy stand-point. Sustainable Materials and Technologies 29, e00296. 2021. https://doi.org/10.1016/j.
Denofrio MP, Rasse-Suriani FAO, Paredes JM, Fassetta F, Crovetto L, Giron MD, Salto R, Epe B, Cabrerizo FM. N-Methyl-β-carboline alkaloids: structure-dependent photosensitizing properties and localization in subcellular domains. Organic and Biomolecular Chemistry 18, 6519-6530. 2020. https://doi.org/10.1039/D0OB01122C
Madriz L, Tatá J, Carvajal D, Núñez O, Scharifker BR, Mostany J, Borrás C, Cabrerizo FM, Vargas, R. Photocatalysis and photoelectrochemical glucose oxidation on Bi2WO6: Conditions for the concomitant H2 production. Renew Energ 152, 974-983. 2020. https://doi.org/10.1016/j.renene.2020.01.071
Torres D, Madriz L, Vargas R, Scharikfer BR. Electrochemical formation of copper phosphide from aqueous solutions of Cu(II) and hypophosphite ions. Electrochimica Acta 354, 136705. 2020. https://doi.org/10.1016/j.electacta.2020.136705
Vargas R, Cabrerizo FM, Hojamberdiev M. FOREWORD: Perspectives of TWAS Young Affiliates from the Global South on Solving World’s Energy Issues. Energy Rep. 6, 1. 2020. https://doi.org/10.1016/j.egyr.2019.11.154
Villarruel FD, Denofrio MP, Erra-Balsells R, Wolcan E, Cabrerizo FM. Photophysical and spectroscopic features of 3,4-dihydro-β-carbolines: a combined experimental and theoretical approach. Physical Chemistry Chemical Physics 22, 20901-20913. 2020. https://doi.org/10.1039/D0CP03363D
Yañuk JG, Cabrerizo FM, Dellatorre FG, Cerdá MF. Photosensitizing role of R-phycoerythrin red protein and β-carboline alkaloids in Dye sensitized solar cell. Electrochemical and spectroscopic characterization. Energy Rep. 6, 25-36. 2020. https://doi.org/10.1016/j.egyr.2019.10.045
Zucchelli M, Villarruel FV, Gara PD, Costante MR, Tascon M, Marte F, GarcíaEinschlag FS, Cabrerizo FM, Photophysics and photochemistry of carminic acid and related natural pigments. Physical Chemistry Chemical Physics 22, 9534-9542. 2020. https://doi.org/10.1039/D0CP01312A
Villarruel F, Denofrio MP, Rasse-Suriani FAO, García Einschlag FS, Schmidt De León T, Erra-Balsells R, Cabrerizo FM. Light-induced full aromatization and hydroxylation of 7-methoxy-1-methyl-3,4-dihydro-2H-pyrido[3,4-b]indole alkaloid: Oxygen partial pressure as a key modulator of the photoproducts distribution. J Photochem Photobiol B. 199: 111600. 2019. https://doi.org/10.1016/j.jphotobiol.2019.111600
Yañuk JG, Cabrerizo FM, Dellatorre FG, Cerdá MF. Photosensitizing role of R-phycoerythrin red protein and ß-carboline alkaloids in Dye sensitized solar cell. Electrochemical and spectroscopic characterization. Energy Rep. 2019. En prensa. https://doi.org/10.1016/j.egyr.2019.10.045


